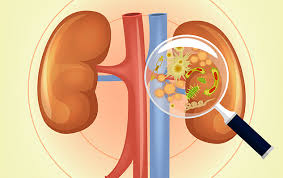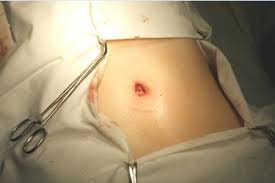
Омфалит — это инфекция пупочной культи. Процесс, как правило, представлен как поверхностный целлюлит (острое воспаление подкожной жировой клетчатки), который способен распространиться на всю брюшную стенку с прогрессом в некротический фасциит, мионекроз или системное заболевание. Омфалит очень редкое явление в промышленно развитых странах. Но проблема остается распространенной причиной смертности новорожденных в менее развитых регионах. Преимущественно болезнь поражает новорожденных, и только несколько случаев зафиксировано у взрослых.
Причины возникновения омфалита у новорожденных и его классификация
Примерно три четверти случаев омфалита имеют полимикробное происхождение. Аэробные бактерии присутствуют примерно в 85 % случаев инфекционных процессов с преобладанием золотистого стафилококка, группы стрептококков А, кишечной палочки, клебсиелл и протея. В прошлом в исследованиях подчеркивалась важность в этиологии омфалита грамположительных микроорганизмов, например, представителей стафилококков и стрептококков.
Позже появилось множество результатов о важной роли грамотрицательных микроорганизмов. Исследования показали, что изменения в этиологии, возможно, были вызваны введением профилактической помощи с использованием пуповинного антистафилококкового агента, такого как гексахлорфен. Эта практика была широко распространена в середине XX века. Видимо, именно такой подход обеспечил последующее увеличение грамм-отрицательных колонизаций пупочной культи.
Как уже отмечалось, омфалит является полимикробной инфекцией, как правило, обусловленной смесью аэробных и анаэробных микроорганизмов.
- Низкий вес при рождении — менее 2500 г.
- Несвоевременное отсечение пуповины.
- Обсеменение хирургической раны культи, что часто возникает в связи с преждевременным разрывом плодных оболочек, нестерильной обработкой раны или материнской инфекцией.
- Длительный разрыв внутренних слоев пуповины.
Омфалит иногда проявляется по причине базового иммунологического расстройства. Дефицит адгезии лейкоцитов является наиболее известным среди иммунодефицитных синдромов. Множество детей с острым или хроническим омфалитом были с подобным диагнозом — редким иммунологическим расстройством аутосомно-рецессивного наследования. Эти дети, как правило, представляют конкретный симптомокомплекс.
- Лейкоцитоз.
- Задержка отделения пуповины с наличием или без омфалита.
- Рецидивирующие инфекции.
Омфалит также может стать начальным проявлением нейтропении у новорожденных. Дети с неонатальной аллоиммунной или врожденной нейтропенией показывают омфалит несколько чаще.
Реже могут присутствовать анатомические аномалии, такие как дефекты мочевого протока или киста мочевого пузыря.
Основы патофизиологии и эпидемиологии
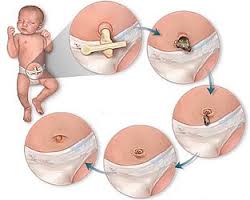
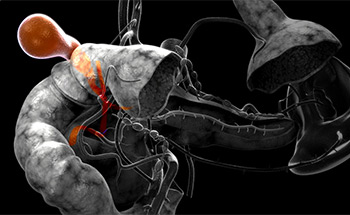
Пуповина соединяет плод с матерью в период внутриутробного развития. Орган состоит из соединительной ткани и кровеносных сосудов. Пуповину отсекают сразу после рождения, оставляя пупочную культю. Как правило, площадь разреза колонизируется потенциальными бактериальными патогенами во время появления на свет или вскоре после рождения. Эти бактерии привлекают лейкоциты, обеспечивающие иммунную защиту. Хотя точные механизмы неизвестны, приток гранулоцитов и фагоцитоз, а также высыхание и последующий некроз на фоне активности коллагеназы и других протеаз вносят свой вклад в процесс.
Пупочная культя представляет собой уникальную рану, ткани которой подвергаются девитализации, этим обеспечивая среду, которая поддерживает рост бактерий. Эти бактерии обладают потенциалом вторжения в пупочную культю, это и приводит к омфалиту. Если это происходит, инфекция может прогрессировать за подкожные ткани, стимулируя развитие некротического фасциита, мионекроз брюшной мускулатуры при проникновении бактерий в пупочные сосуды и портальные вены. Факторы, которые вызывают активизацию инфекции, не очень хорошо изучены.
В целом заболеваемость омфалитом колеблется от 0,2 до 0,7 % в промышленно развитых странах. Уровень заболеваемости обычно выше у госпитализированных недоношенных детей. Эпизоды омфалита, как правило, носят спорадический характер. Эпидемии крайне редки, и вызываются они, например, золотистым стафилококком или группой стрептококков.
- Прогноз, как правило, благоприятный у детей с неосложненной формой омфалита, связанной с целлюлитом передней брюшной стенки.
- Смертность значительно выше — 38-87 % после развития некротического фасциита или мионекроза.
Предлагаемые факторы риска для неблагоприятного прогноза также включают в себя мужской пол, недоношенность и плохую обработку пупочной культи. Однако данные в этой области ограничены, и выводы не могут быть сделаны в отношении роли приведенных факторов в смертности.
Осложнения омфалита могут быть связаны с высокой заболеваемостью и смертностью. Они включают в себя ряд моментов.
- Некротический фасциит.
- Мионекроз.
- Сепсис.
- Септическую эмболизацию.
- Эндокардит.
- Абсцесс печени по причине формирования брюшных осложнений.
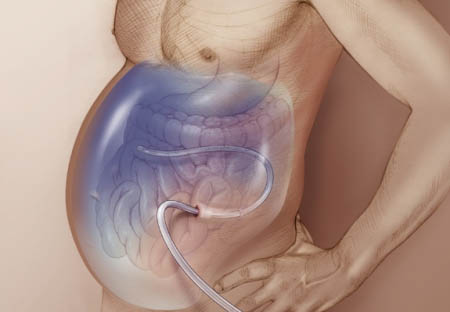
- В самых тяжелых случаях это могут быть перитонит, непроходимость кишечника или забрюшинный абсцесс и смерть.
Некротический фасциит — это бактериальная инфекция кожи, подкожно-жировой клетчатки с вовлечением поверхностной и глубокой фасции, что осложняет 8-16 % случаев неонатального омфалита. Заболевание характеризуется быстрым распространением инфекции и тяжелой системной токсичности. Некротический фасциит, как правило, поражает брюшную стенку, может распространяться на мошонку или половой член.
Некротическая инфекция мягких тканей влечет за собой непосредственно клеточную гибель, ферментативное разрушение поддерживающих соединительно-тканных структур и подавление гуморальной и клеточной иммунной реакции организма.
Роль некоторых микроорганизмов хорошо изучена в развитии некротических процессов. Стрептококки, золотистый стафилококк и виды клостридий вырабатывают внеклеточные ферменты и токсины, которые могут повредить ткань. И это дополнительно способствует продвижению патогенов в глубжележащие структуры.
У детей с омфалитом развитие мионекроза обычно зависит от условий, которые способствуют росту анаэробных организмов. Эти условия включают в себя наличие некротических тканей, плохое кровоснабжение, чужеродный материал и наличие аэробных бактерий, таки как стафилококки или стрептококки. Токсины, произведенные в анаэробной среде некротических тканей, позволяют быстро распространяться микроорганизмам через ткани брюшной стенки.
Местное распространение токсинов расширяет область некроза тканей, что стимулирует дальнейший рост колоний патогенных представителей и повышение выработки токсинов. Анаэробные инфекции из-за прогрессирующей деструкции тканей и глубокого последующего системного распространения токсинов становятся смертельными, если их своевременно не подвергнуть лечению. Кроме того, быстрое развитие отека, который сжимает мышцы и фасции, может привести к ишемическому мионекрозу.
Сепсис — наиболее частое осложнение омфалита. Источником септической эмболизации становятся пораженные сосуды пуповины. Это может вызвать метастатическое распространение в различные органы, в том числе в сердце, печень, легкие, поджелудочную железу, почки и кожу.
Какие бывают брюшные осложнения?
- Перитонит.
- Непроходимость кишечника.
- Брюшной абсцесс.
- Абсцесс печени.
Долгосрочные или поздние осложнения омфалита могут включать в себя неопухолевые кавернозные преобразования воротной вены, портальный тромбоз, внепеченочную портальную гипертензию и обструкцию желчных путей.
Если говорить о гендерной принадлежности заболевания, то она не наблюдается. Хотя младенцы мужского пола могут иметь худший прогноз. У доношенных детей, средний возраст начала заболевания — 5-9 дней, у недоношенных — 3-5.
Симптомы воспаления пупка у детей, и в чем опасность гнойного омфалита?
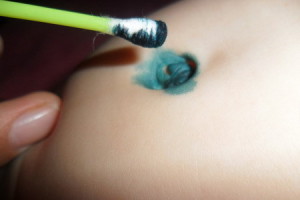
Физические признаки омфалита варьируются, в зависимости от степени заболевания.
- Гнойные или зловонные выделения из пупочной культи.
- Эритема в пупочной области.
- Отек.
- Повышенная чувствительность.
Есть признаки, указывающие на более обширное течение местного заболевания и плавно переходящие в осложнения, такие как некротический фасциит или мионекроз, которые обычно локализуются вокруг пупка, но могут распространиться по всей брюшной стенке, по бокам и паховую область. Эти признаки могут также указывать на аэробную и анаэробную инфекции.
- Синяки фиалкового цвета.
- Буллы.
- Крепитация.
- Петехии.
- Прогрессирование целлюлита, несмотря на антимикробную терапию.
Признаки сепсиса или других системных заболеваний являются неспецифическими. Они включают в себя нарушения терморегуляции или доказательства дисфункции различных систем и органов.
- Нарушения терморегуляции — лихорадка с температурой более 38 °С) или гипотермия — температура тела менее 36 °С). Часто возможны резкие перепады из одного состояния в другое.
- Сердечно-сосудистые нарушения — тахикардия с пульсом более 180 ударов в минуту, артериальная гипотензия — систолическое артериальное давление менее 60 мм рт. ст. у доношенных детей, задержка наполнения капилляров.
- Респираторные нарушения — апноэ, тахипноэ — более 60 дыхательных движений в минуту, гипоксемия.
- Пищеварительные расстройства — жесткий или растянутый живот, отсутствие звуков перистальтики кишечника.
- Кожные проявления — желтуха, петехии или цианоз.
- Неврологические нарушения — раздражительность, вялость, слабое сосание, гипотония, сонливость, чередующаяся с криком и плачем.
Диагностика и лечение воспаления пупочной ранки
Бактериологические лабораторные исследования проводят регулярно на образцах пуповинной инфекции. Бакисследование включает в себя классическую окраску по Граму с целью определения принадлежности возбудителей к аэробному или анаэробному типу. Если подозревается мионекроз, понадобятся образцы из пораженной мышцы, а не раневой поверхности пупочной культи.
Нейтрофилез или нейтропения могут присутствовать при острой инфекции. Отношение незрелых нейтрофилов, как правило, выше в 0,2 раза к общему количеству. И это может стать полезным индикатором системной бактериальной инфекции в первые дни жизни. Тромбоцитопения также может присутствовать.
Другие не специфические лабораторные тесты, проводимые по отдельности или в сочетании, проводят по специальным схемам. Однако их полезность может не быть достаточно высокой для того, чтобы определять клиническое лечение. Тесты включают в себя ряд моментов.
Уровни С-реактивного белка в сыворотке крови:
- концентрации прокальцитонина;
- скорость оседания эритроцитов;
- лейкоформула;
- различные методы обнаружения эндотоксинов.
Следующие лабораторные исследования могут быть применены у новорожденных, у которых наблюдаются признаки сепсиса и диссеминированного внутрисосудистого свертывания.
- Мазок периферической крови.
- Протромбиновое время.
- Активированное частичное тромбопластиновое время.
- Фибриноген.
- D-димер.
Другие аномалии, связанные с серьезной системной инфекцией, могут показать:
- гипогликемию.
- гипокальциемию, часто связанную с омылением жирных кислот с помощью бактериальных липаз в подкожной ткани;
- метаболический ацидоз.
- Брюшная рентгенография может выявить наличие внутрибрюшного газа.
- УЗИ может определить накопление фасциальной жидкости и подкожного жира между мышцами и фасциями. Метод также может быть полезным в обнаружении анатомических аномалий.
- Компьютерная томография брюшной полости может определить наличие и степень вовлечения мышц и фасций, а также потенциально помочь в обнаружении анатомических аномалий.
Гистологический анализ образца биопсии может выявить некротический фасциит, находящийся в стадии острого воспалительного инфильтрата в подкожной жировой и соединительной ткани, либо мионекроз, окружающий мышечные пучки, многие из которых более не являются жизнеспособными.
Лечение омфалита у новорожденных включает в себя, как правило, антимикробную и поддерживающую терапию. При антимикробной терапии обращают внимание на некоторые моменты.
Обязательное парентеральное антимикробное покрытие для грамположительных и грамотрицательных микроорганизмов. Для этого рекомендовано сочетание антистафилококкового пенициллина, ванкомицина и аминогликозидов.
Омфалит, осложненный некротическим фасциитом или мионекрозом, требует более агрессивного терапевтического подхода антимикробной терапии, направленной на анаэробные организмы, а также грамположительные и грамотрицательные агенты. Метронидазол или клиндамицин вполне способны обеспечить анаэробные покрытие. Обязательно следует учитывать возможную устойчивость золотистого стафилококка и энтерококков.
Дополнительное местное лечение с применением бацитрацина и других противомикробных препаратов было предложено в дополнение к парентеральной терапии антибиотиками, но такое лечение не доказано.
Как дополнение к антибактериальной терапии, поддерживающая терапия играет важную роль для выживания.
- Обеспечение вентиляционной помощи и дополнительного кислорода для предотвращения гипоксемии или апноэ.
- Применение вазоактивных агентов при гипотонии.
- Назначение свежезамороженной плазмы, криопреципитата или факторов диссеминированного внутрисосудистого свертывания.
- Лечение детей проводить в центрах, способных поддерживать сердечные функции.
Другие соображения лечения
- Мониторинг пациентов обязателен с целью контроля над прогрессированием заболевания. Раннее хирургическое вмешательство может спасти жизнь.
- В не осложненных случаях эритема пупочной культи может купироваться в течение 12-24 часов после начала антибактериальной терапии. Отсутствие реакции может свидетельствовать о прогрессировании заболевания, наличии анатомического дефекта или состояния иммунодефицита.
Роль гипербарической оксигенации в лечении больных с анаэробным некротическим фасциитом и мионекрозом является спорным, поскольку нет контролируемых данных об эффективности. Доставка высоких концентраций кислорода может оказывать отрицательное воздействие на рост анаэробных организмов и улучшить функцию фагоцитов. Тем не менее, хирургическое лечение и сейчас является наивысшим приоритетом, и инициирование гипербарической кислородной терапии не должно задерживать оперативное лечение.
Лечение некротического фасциита и мионекроза включает в себя раннюю и полную хирургическую обработку пораженной ткани и мышцы.
- Хотя степень санации зависит от жизнеспособности ткани и мышц, что определяется на момент операции, иссечение ткани в предбрюшинной области, в том числе пупка, пупочных сосудов, является критически важным в искоренении инфекции.
- Эти ткани могут питать инвазивные бактерии и обеспечивать маршрут для прогрессивного распространения инфекции после менее обширной хирургической обработки раны.
- Задержка в диагностике или хирургии позволяет развиваться и распространяться некрозу, что приводит к гибели больших областей ткани и повышению уровня системной токсичности.
- Может понадобиться несколько хирургических процедур, прежде чем все нежизнеспособные ткани будут удалены.
После того, как омфалит будет выведен на стадию подозрения, энтеральное кормление запрещено. Процесс можно возобновить, как только острая инфекция будет исключена. В остальных случаях необходимо обеспечить строго парентеральное введение питательных сред.